孙佳琦1,2,曹燕亭1,2,吕雪芹1,2,李江华1,2,刘龙1,2,堵国成1,2,陈坚1,2,刘延峰1,2*
1 江南大学生物工程学院 糖化学与生物技术教育部重点实验室,江苏 无锡 214122
2 江南大学未来食品科学中心,江苏 无锡 214122
摘要:枯草芽孢杆菌(Bacillus subtilis)是公认的食品安全菌株,目前已被用于多种高附加值产品的生物合成,包括被广泛用作营养化学品和药物中间体的 N-乙酰神经氨酸(N-acetylneuraminic acid, Neu Ac)。响应目标产物的生物传感器被广泛用于代谢工程中的动态调控和高通量筛选等方面,以提高生物合成效率。但是,枯草芽孢杆菌中缺乏可高效响应 Neu Ac 的生物传感器。因此,本文首先测试和优化了能将胞外 Neu Ac 转运进胞内的转运蛋白,获得了一系列具有不同转运能力的菌株,以用于后续响应 Neu Ac 的生物传感器的验证;随后将响应 Neu Ac 的转录因子 Bbr_Nan R 的结合位点插入枯草芽孢杆菌组成型启动子的不同位置,筛选具有活性的杂合启动子;接下来,通过在具有 Neu Ac 转运能力的枯草芽孢杆菌中表达 Bbr_Nan R,选择能响应 Neu Ac 的杂合启动子,并进一步通过优化 Bbr_Nan R 表达量获得了一系列动态范围广、激活倍数高的生物传感器,其中生物传感器 P535-N2 能灵敏地响应胞内 Neu Ac 浓度的变化,具有最大的动态范围,为(180–20 245) AU/OD;P566-N2 则具有最高的激活倍数,为 122 倍,是已报道的枯草芽孢杆菌中响应 N-乙酰神经氨酸的生物传感器的 2 倍。本文构建的响应 Neu Ac 的生物传感器可用于高产 Neu Ac 的酶突变体和枯草芽孢杆菌菌株的筛选,为枯草芽孢杆菌生物合成 Neu Ac 提供了高效、灵敏的分析和调控工具。
关键词:枯草芽孢杆菌;N-乙酰神经氨酸;转录因子;生物传感器
N- 乙酰神经氨酸 (N-acetylneuraminic acid, Neu Ac)又称燕窝酸,是一种带负电荷的功能性单糖,存在于多种动物、植物、微生物中,也是人体中唾液酸的主要存在形式[1]。Neu Ac 不仅是唾液酸化人乳低聚糖的重要单体之一,也是神经节苷脂的传递递质,因此常作为食品添加剂促进婴幼儿的大脑和骨骼发育,有利于维持老年人的大脑健康,减缓老年痴呆症等神经系统疾病的发展[2-4]。此外,Neu Ac 也被应用于药物、疾病治疗等领域[5-6]。由于天然提取法和化学合成法的局限性,目前,N-乙酰神经氨酸更多地用生物合成法获得,主要包括酶法合成、全细胞催化法以及微生物发酵法。其中,酶法合成和全细胞催化都需要添加昂贵的前体物质,造成生产成本的增加,而微生物发酵法可以通过廉价碳源实现 N-乙酰神经氨酸的从头合成,成为最具有潜力的生产策略[1]。
枯草芽孢杆菌(Bacillus subtilis)作为一种革兰氏阳性模式菌株,拥有成熟的基因操作工具,且无内毒素,被美国食品药品监督管理局(Food and Drug Administration, FDA)认证为食品级微生物[7]。在工业生产中,枯草芽孢杆菌因生长迅速、对培养条件要求较低、不易受噬菌体侵染等优势而备受关注,广泛应用于食品、药品、酶制剂等的生产[8-11],是合成 N-乙酰神经氨酸的优良宿主。 生物传感器(biosensor)作为一种重要的合成生物学工具,在细胞工厂中具有多种应用。代谢工程中常用的生物传感器可分为基于 RNA 的核糖开关(riboswitches)和适体酶(aptazymes),以及基于转录因子的传感器[transcription factor (TF)-based biosensors] [12],其中基于转录因子的传感器应用更为广泛,在适应性进化、高活性酶筛选、高产菌株筛选、动态调控、基因型和表型异质性调控等方面都发挥了重要作用[13-17]。Pang 等[18]在大肠杆菌(Escherichia coli)中构建了响应 Neu Ac 的适体酶,基于此开发了生长偶联的筛选策略,并获得了 Neu Ac 产量提高 42%高产菌株。Peters 等[19]在大肠杆菌中构建了基于转录因子的响应 Neu Ac 的生物传感器,并用不同产量的菌株验证了生物传感器作为高通量筛选方法的适用性。目前,基于大肠杆菌来源的 Nan R,Zhang 等[20]在枯草芽孢杆菌中构建了可响应 Neu Ac 的生物传感器,但是其动态范围和灵敏度不高,限制了其在指导 Neu Ac 生产方面的应用。 本 研 究 选 取 短 双 歧 杆 菌 (Bifidobacterium breve) 来源 Nan R (Bbr_Nan R) 在枯草芽孢杆菌中构建了可高效响应 Neu Ac 的生物传感器 。 首先测试和优 化了来源于大肠杆菌的Neu Ac 转运蛋白 Nan T 和Nan C的转运能力,获得了一系列具有不同转运能力的菌株,以用于后续响应Neu Ac的生物传感器的验证;随后,将 Bbr_Nan R 特异性结合序列(Nan R binding site)插入到枯草芽孢杆菌组成型启动子的不同位置,构建了一系列杂合启动子,并用这些杂合启动子调控绿色荧光蛋白(green fluorescent protein, GFP)的表达,选择了一系列有活性的杂合启动子用于后续实验;接下来,通过在具有 Neu Ac 转运能力的枯草芽孢杆菌中表达 Bbr_Nan R,选择能响应 Neu Ac的杂合启动子,并在此基础之上进一步优化Bbr_Nan R 表达量,成功获得了一系列可以在枯草芽孢杆菌中高效响应 Neu Ac 的生物传感器,它们能灵敏地响应胞内 Neu Ac 浓度的变化,且具有更高的动态范围。本文构建的响应 Neu Ac 的生物传感器可用于高产 Neu Ac的酶突变体和枯草芽孢杆菌菌株的筛选,为枯草芽孢杆菌生物合成 Neu Ac 提供了高效、灵敏的分析和调控工具。
1 材料与方法
1.1 材料
1.1.1 菌株和质粒
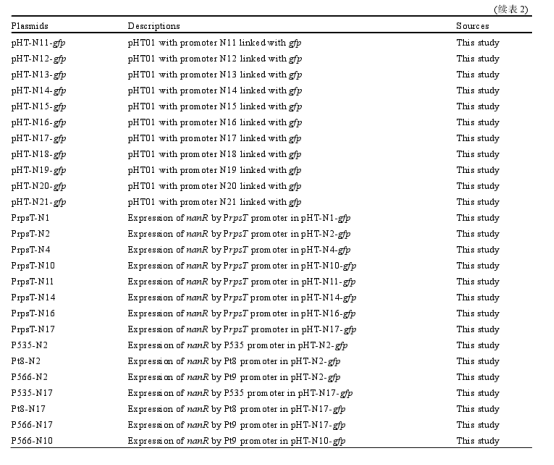
本研究所用初始菌株与质粒均为实验室保藏。详细信息见表 1 和表 2。


1.1.2 培养基
LB 培养基:5 g/L 酵母粉,10 g/L 蛋白胨,10 g/L Na Cl,固体培养基添加 20 g/L 的琼脂粉。根据需要添加相应浓度的抗生素(氯霉素终浓度为 5 mg/L,壮观霉素终浓度为 100 mg/L,氨苄霉素终浓度为 100 mg/L)。
1.1.3 主要试剂
Prime Star max 聚合酶购于 Ta Ka Ra 公司;质粒提取、感受态制备试剂盒购于生工生物工程(上海)股份有限公司;Gene JET PCR 纯化试剂盒购于 Thermo Scientific 公司。
1.2 方法 基因序列与引物合成
将 NCBI 数据库中 B. breve UCC2003 来源Nan R 的氨基酸序列送至苏州金唯智公司进行密码子优化(表达宿主:Bacillus subtilis 168)并合成,Bbr_Nan R 结合位点参考 Egan 等[21]的报道。文中所有引物的合成和测序反应均由苏州金唯智生物科技有限公司或者生工生物工程(上海)股份有限公司(以下简称“上海生工”)完成,本文部分引物信息见表 3,更换启动子所用引物根据表 4 启动子序列进行设计。

1.2.2 重组菌株的构建
BS-nan C、BS-nan T 的构建:以 B. subtilis 168基因组为模板,通过聚合酶链式反应(polymerasechain reaction, PCR)扩增 ydb D 位点上下游各1 000 bp 的序列作为左右同源臂,以 E. coli JM109 基因组为模板,扩增 nan C、nan T 基因,以实验室保存质粒 p7S6P43[7]为模板扩增壮观 霉素抗性框和 P43 启动子片段。通过融合 PCR将左右臂、抗性框和 P43 启动子片段、nan C (nan T)片段进行融合,获得基因 nan C (nan T)的表达框,并转化枯草芽孢杆菌 BSXC 感受态,获得菌株 BS-nan C (BS-nan T)。 BSP1–BSP10 的构建:左右臂和 nan T 片段参考上述方法获得,以实验室保存的 p7S6P1

系列质粒[22]为模板扩增获得壮观霉素抗性框和启动子片段,然后按照上述 BS-nan T 的构建方法得到重组菌株 BSP1–BSP10。
1.2.3 重组质粒的构建
杂 合 启 动 子 重 组 质 粒 的 构 建 : 以 p HT- veg-gfp 为模板,用相应的引物进行扩增获得带有杂合启动子的线性质粒片段,上下游引物包括杂合启动子序列、特异性结合序列,且存在一段 20 bp 左右的重叠(overlap)。利用 Thermo Scientific Gene JET PCR 纯化试剂盒对所获得的线性质粒片段进行纯化,然后取 10 μL 转化E. coli JM109 感受态,并涂布抗性平板。次日将平板上的单菌落送上海生工测序,将测序正确的单菌落扩大培养,并提取重组质粒。优化nan R 表达量时,也采用同样的环化 PCR 的方式替换 nan R 的启动子。
生物传感器重组质粒的构建:分别以杂合启动子重组质粒为模板,用引物 p N-F/R 扩增质粒骨架及杂合启动子表达的绿色荧光蛋白基因gfp,以 p HT-nan R 为模板,用引物 nan R-F/R 扩增 Prps T 启动子表达的 nan R 基因,利用 Thermo Scientific Gene JET PCR 纯化试剂盒将所得片段纯化,经 Gibson 组装[23]后转化 E. coli JM109感受态,并涂布抗性平板。次日将平板上的单菌落送上海生工测序,将测序正确的单菌落扩大培养,并提取重组质粒。
1.2.4 感受态细胞的制备和转化
大肠杆菌感受态制备与转化:超级感受态细胞制备试剂盒购于生工生物工程(上海)股份有限公司,按照说明书要求制备、转化E. coli JM109 感受态细胞,用于质粒的构建。 枯草芽孢杆菌感受态制备与转化:参考Zhang 等[24]的方法,在 B. subtilis 168 基因组上整合了一个受木糖诱导型启动子Pxyl A调控的com K基因,得到菌株BSXC作为本研究的出发菌株,利用木糖诱导制备感受态细胞。挑取平板活化的B. subtilis 单菌落在1mL LB 培养基中于 37℃、220 r/min 的条件下培养 12h,加入LB 培养基稀释至5mL,并加入终浓度为 3%的木糖,于 37℃、220 r/min 条件下诱导 2 h 后获得感受态。将适量的质粒或片段加入100 µLB. subtilis 感受态细胞,于37℃、220 r/min的条件下培养 1.5 h后涂布相应抗性平板,置于37℃恒温培养箱培养。
1.2.5 胞内 Neu Ac 浓度检测
胞内 Neu Ac 测定样品制备:取1 m L发酵液,置于预冷为4℃的离心机,6 000 r/min 离心 5 min,弃尽上清液,将菌体重悬于 1 m L 预冷的无菌水中洗涤1次,6 000 r/min 离心 5 min,弃尽上清液,用 0.2 m L 无菌水重悬菌体,后加入0.4 m L乙腈和 0.4 m L甲醇混匀,并置于–20 ℃过夜萃取。将萃取液于4℃、12 000 r/min 离心10 min,上清液置于冷冻干燥机过夜干燥。干燥后的粉末重悬于一定体积的无菌水以浓缩样品,用于高效液相色谱检测。 高效液相色谱(high performance liquid chromatography, HPLC) 检测:取样品通过0.22μm 的滤膜,采用 Aminex HPX-87H 柱 (300 nm×7.8 nm)进行 HPLC 检测,检测参数如下:采用10 mmol/L H2SO4作为流动相,0.5 m L/min流速进样,进样量为10μL,柱温为40 ℃,紫外检测器波长为210 nm。
1.2.6 GFP 荧光强度检测方法
将培养过夜的种子液以 2%转接到含有 0.2 mL LB 培养基的 96 浅孔板中,37 ℃、900 r/min 培养 8h,用酶标仪在490nm 的激发波长、530nm的发射波长和 60 的增益值下测定 GFP的荧光强度;在 600nm 的波长下测定 OD600。减去培养基的背景噪声后,计算荧光强度与OD600的比值,再减去无GFP 表达的对照菌株的荧光强 度与OD600的比值,即得到相对荧光强度。
2 结果与分析
2.1 Neu Ac 转运蛋白 Nan T 和 Nan C 的测试和表达优化
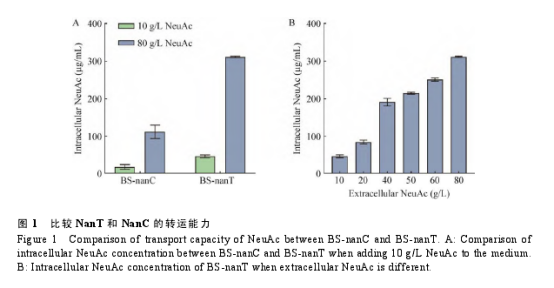
在响应小分子代谢物的生物传感器构建过程中,常常采用在培养基中添加不同浓度的小分子代谢物来验证生物传感器的响应性能,而枯草芽孢杆菌不具备将胞外 Neu Ac 转运进胞内的能力,因此,首先需要构建能将胞外 Neu Ac转运进胞内的枯草芽孢杆菌,便于外源添加Neu Ac 以验证生物传感器的性能。为了不影响内源基因的表达,选择 ydb C 和 ydb D 基因的间隔位置作为基因组整合表达 nan C 和 nan T 的位点。按照方法 1.1.2,将由 P43 启动子调控 nan C (nan T)的表达框整合到枯草芽孢杆菌 BSXC 的基因组,得到菌株 BS-nan C (BS-nan T)。为了比较 Nan C 和 Nan T 转运 Neu Ac 的能力,将菌株 BS-nan C 和 BS-nan T 分别在添加了 10g/L和 80g/L Neu Ac 的 LB 培养基中发酵 12h,随后检测其胞内 Neu Ac 含量。
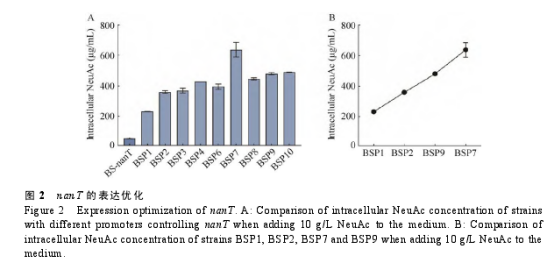
与 BS-nan C 相比,BS-nan T 转运 Neu Ac 的能力更强,且外源添加不同浓度的 Neu Ac 时胞内浓度差异较大,是验证响应 Neu Ac 的生物传感器的更优宿主(图 1A)。BS-nan T 在外源添加10–80 g/L Neu Ac 的 LB 培养基中发酵 12 h 时,胞内 Neu Ac 浓度也存在差异,但是胞内 Neu Ac浓度总体偏低,最高也只有 310 μg/m L (图 1B),这不利于对响应 Neu Ac 浓度范围广的生物传感器的验证,于是进一步对 nan T 进行表达优化。选取枯草芽孢杆菌中 9 个不同强度的内源启动子(P1、P2、P3、P4、P6、P7、P8、P9 和 P10)[22]替换 P43 启动子调控 nan T 的表达,得到菌株BSP1–BSP10。如图 2 所示,当在添加了 10 g/L Neu Ac 的 LB 培养基中发酵 12 h 时,菌株BSP1–BSP10 的胞内 Neu Ac 含量在 230–635 μg/m L之间变化。其中,BSP1、BSP2、BSP7 和 BSP9之间的胞内 Neu Ac含量差异显著,且胞内 Neu Ac浓度范围更广(230–635 μg/m L),可用于后续响应 Neu Ac 生物传感器的性能验证。
2.2 响应 Neu Ac 生物传感器的设计与构建
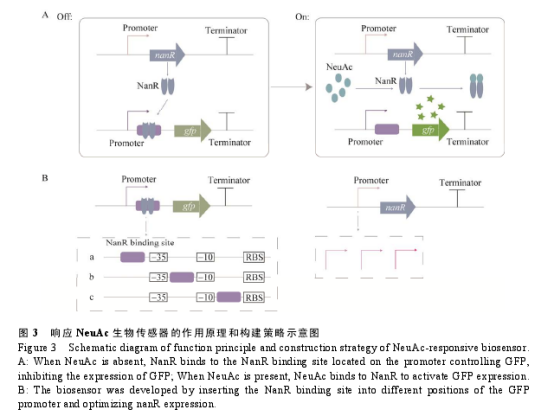
基于转录因子的生物传感器通常包括 3 个部分:响应特定代谢物的转录因子,含有转录因子结合位点的启动子以及受其调控表达的报告基因[25-26]。响应 Neu Ac 生物传感器的原理如图 3A 所示,当胞内不存在 Neu Ac 时,Bbr_Nan R作为阻遏蛋白结合在其结合位点上,抑制响应启动子调控的报告基因的表达;当胞内存在Neu Ac 时,胞内 Neu Ac 与 Bbr_Nan R 的结合会影响 Bbr_Nan R 的阻遏活性,从而激活响应启动子的表达。
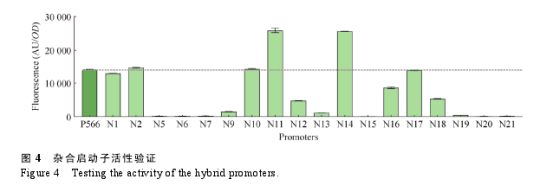
因此,首先设计了含有 Nan R 结合位点的杂合启动子。如图 3B 所示,将 Bbr_Nan R 特异性结合位点放在了 6 个组成型启动子 Pveg、P43、Pm1、P214、P566、P535[27-28]的–35 区前、–35 区和–10 区中间、–10 区后,设计了 21 个带有 Bbr_Nan R 结合位点的杂合启动子 N1–N21 (序列如表 4 所示)。以 p HT01 质粒为载体,分别用杂合启动子表达 GFP,将构建成功的质粒转化 BS-nan T 菌株以检测杂合启动子活性。如图 4 所示,虽然大多数杂合启动子在插入 Nan R的结合序列后活性明显降低甚至失去活性,但是杂合启动子 N1、N2、N10、N11、N14、N16、N17 显示出了接近甚至超过强组成型启动子P566 的活性,因此,选择这些杂合启动子用于后续响应 Neu Ac 生物传感器的构建。
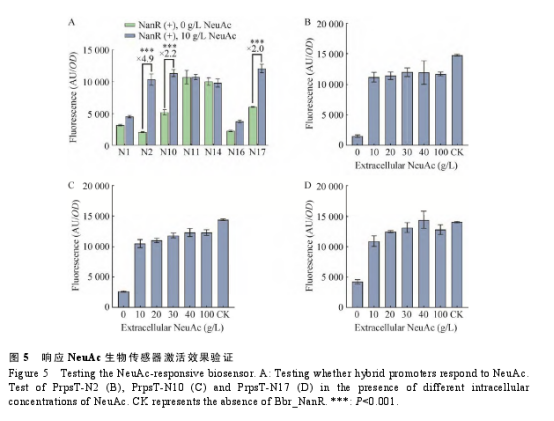
为了验证这些高活性的杂合启动子能否被Bbr_Nan R抑制,能否被 Neu Ac 激活,在杂合启动子调控GFP表达框的上游引入 Prps T 启动子表达的 nan R,然后将构建成功的 7 个生物传感器质粒转入BS-nan T,发现当不添加 Neu Ac时,杂合启动子 N1、N2、N10、N16 和 N17 能被一定程度地抑制;当外源添加 10 g/L Neu Ac时,这几个杂合启动子也能被激活(图 5A)。其中 N2、N10 和N17能被激活至少2倍,这有利于灵敏地响应低浓度的胞内 Neu Ac。因此,选择了这几个杂合启动子进行后续实验。接下来分析了外源添加不同浓度的Neu Ac时杂合启动子N2、N10、N17 的表达情况,如图5B–5D所示,虽然它们都能被激活,但是当胞外添加 10 g/L 的Neu Ac (低浓度)时它们的表达强度已接近杂合启动子被完全激活的强度,因此,推测nan R 的表达量不足以用于响应更高浓度的胞内 Neu Ac,并利用不同强度的启动子优化nan R表达。
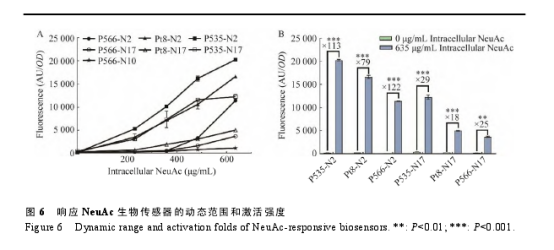
在2.1中,研究发现当外源添加10 g/L 的Neu Ac 时,菌株 BSP1、BSP2、BSP9、BSP7的胞内 Neu Ac 浓度在 230–635 μg/m L 范围内存在显著差异。为了能获得响应 Neu Ac 浓度范围广且灵敏的生物传感器,后续选择这4株菌去验证生物传感器对不同浓度 Neu Ac 的响应效果。分别选取 N2、N10 和 N17 启动子表达 GFP,在此基础上选取3个不同强度的启动子 P535、 Pt8、P566 优化 nan R 的表达。将构建成功的重组质粒 P535-N2、Pt8-N2、P566-N2、P566-N10、P535-N17、Pt8-N17、P566-N17 分别转入菌株BSP1、BSP2、BSP7、BSP9 中。当外源添加10 g/L 的 Neu Ac 时,发现 P566-N10 虽然能够响应 Neu Ac,但是激活后的杂合启动子活性远远小于无 nan R 存在时杂合启动子的活性,对此,推测 nan R 的表达量太高,P566-N10 可能需要更高浓度的胞内 Neu Ac 才能被更高强度地激活。除 P566-N10 外的 6 个生物传感器都可以灵敏地响应 Neu Ac,且激活强度可达到 18–122 倍(图 6)。其中 P535-N2 响应 Neu Ac 的动态范围最广,为(180–20 245) AU/OD;P566-N2 响应Neu Ac 的激活强度最大,为 122 倍,为已报道的枯草芽孢杆菌中响应 Neu Ac 的生物传感器[20]的 2 倍。此外,本文只是在胞内 Neu Ac 浓度为0–635 μg/mL 的范围内对几个生物传感器进行了验证,635 μg/m L 的胞内 Neu Ac 浓度并未使P535-N2、Pt8-N2 和 P566-N2 达到饱和状态, 因此,这3个生物传感器响应的 Neu Ac 浓度范围可能比所使用的 0–635μg/m L 范围更广,可以用于分析和检测更高浓度的胞内 Neu Ac。
3 讨论与结论
N-乙酰神经氨酸由于在食品和医药等方面的广泛应用及潜在价值而备受关注,枯草芽孢杆菌作为食品安全级模式微生物,是生产 Neu Ac的理想宿主。目前,Zhang 等[22]以枯草芽孢杆 菌作为宿主菌株生产 Neu Ac,使用葡萄糖作为唯一碳源,在 5L 发酵罐中分批补料发酵,Neu Ac 产量达到 30.10g/L。然而,枯草芽孢杆菌中 Neu Ac 合成途径的改造存在细胞生长与产物生产不平衡、中间产物过度积累等一系列问题,限制了 Neu Ac 的高效合成。响应目标产物的生物传感器常结合流式细胞术实现其在高通量筛选中的应用,也常用于基因回路的设计以构建智能细胞工厂,提高生物合成效率。虽然本研究构建的响应 Neu Ac 的生物传感器响应的是胞内 Neu Ac 浓度变化,但是目前已有越来越多的研究结合这种生物传感器和流式细胞仪来进行高通量筛选,并获得了胞外目标产物产量增加的菌株,证实了这类生物传感器在高产菌株筛选中的应用潜力[16,18,29-30]。另外,本文发现当在枯草芽孢杆菌中适量表达大肠杆菌来源的Nan T 时,不同的胞外 Neu Ac 浓度会导致不同的胞内 Neu Ac 浓度。因此,结合基于液滴微流控的共培养,构建的响应胞内 Neu Ac 的生物传感器也可用于胞外Neu Ac 产量增加的菌株的高通量筛选。构建用于枯草芽孢杆菌的高效响应Neu Ac 的生物传感器,对于指导 Neu Ac 的合成具有重要意义。
本研究首先引入大肠杆菌来源的 Neu Ac 转运蛋白 Nan T,并选取10个不同强度的启动子对其进行表达优化,获得4株具有不同 Neu Ac转运能力的枯草芽孢杆菌作为响应 Neu Ac 生物传感器的验证宿主。然后选取6个组成型启动子,分别在其不同区域插入 Bbr_Nan R 结合位点并验证活性,获得了7个有活性的杂合启动子,在此基础上进一步引入和优化 Bbr_Nan R的表达,得到了6个能够高效响应 Neu Ac 的生物传感器。其中 P535-N2 具有最广的动态范围,为(180–20 245) AU/OD;P566-N2 的激活倍数最高,可达 122 倍,为枯草芽孢杆菌中已报道的响应 Neu Ac 生物传感器[20]的2倍。
本研究侧重对响应 Neu Ac 生物传感器的构建及响应性能的验证,在后续的研究中,可以通过增加胞内 Neu Ac 浓度进一步探究生物传感器的动态范围。此外,本研究构建的生物传感器可结合流式细胞仪应用于枯草芽孢杆菌中Neu Ac 合成途径的高活性酶突变体及高产菌的筛选、群体质量控制等,为枯草芽孢杆菌进一步高效生产 Neu Ac 奠定了基础。
